1- La Teoría cinética molecular
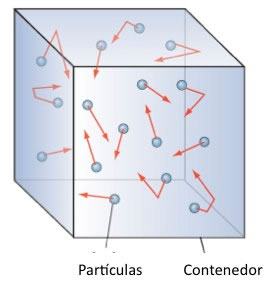
A lo largo de la historia, se desarrolló un modelo sobre la constitución de la materia llamado Modelo Cinético Molecular. Según este modelo, la materia está formada por partículas diminutas llamadas moléculas. Estas se mantienen unidas por fuerzas de atracción y están en constante movimiento gracias a la energía cinética que poseen.
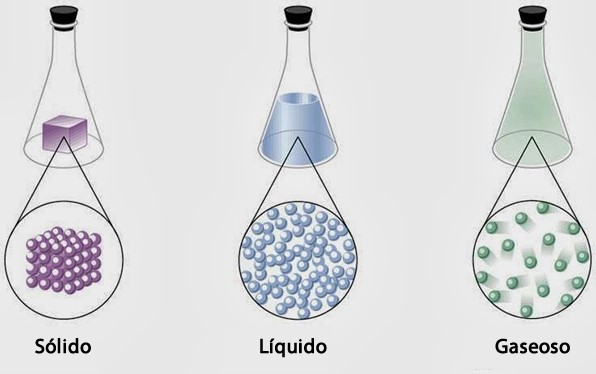
La materia se presenta en tres estados físicos: sólido, líquido y gaseoso.
En el estado sólido, las moléculas están muy juntas debido a fuertes fuerzas de atracción. Permanecen en su lugar y solo vibran.
En el estado líquido, las moléculas están más separadas y se mueven con mayor libertad. Cambian de posición recorriendo distancias cortas. Las fuerzas de atracción son menores que en los sólidos.
En los gases, las moléculas se mueven libremente porque casi no hay fuerzas de atracción entre ellas. Por eso se desplazan en todas direcciones.
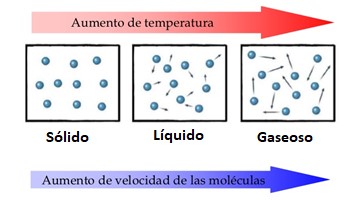
El modelo también señala que al aumentar la temperatura, aumenta la velocidad de las moléculas debido a su energía cinética.
El movimiento constante de las moléculas gaseosas llamó la atención de científicos desde el siglo XVIII. A través de experimentos, se desarrolló un modelo para explicar el comportamiento de los gases: la teoría cinético-molecular de los gases.
2- Teoría cinético-molecular de los gases
En 1738, Daniel Bernoulli aplicó las leyes del movimiento de Newton a las moléculas y dedujo la Ley de Boyle. Sin embargo, su trabajo pasó desapercibido por más de un siglo.
Más adelante, los experimentos de Joule demostraron que el calor es una forma de energía. Esto impulsó nuevamente las ideas de Bernoulli. Entre 1848 y 1898, científicos como Joule, Clausius, Maxwell y Boltzmann desarrollaron la teoría cinético-molecular, también llamada teoría cinética de los gases. Esta propone que todos los gases se comportan de forma similar en cuanto al movimiento de sus moléculas.
En 1905, Einstein aplicó esta teoría al movimiento browniano. Sus fórmulas fueron confirmadas por Perrin en 1908, convenciendo a los escépticos de la existencia de los átomos.
1.1- ¿Qué plantea la teoría cinético-molecular?
Esta teoría explica el comportamiento de los gases mediante los siguientes postulados:
- Los gases están formados por moléculas con masa que se mueven de forma aleatoria y continua.
- Las partículas están en constante movimiento y chocan entre sí y contra las paredes del recipiente. Poseen energía cinética, y los choques son elásticos, es decir, no pierden energía.
- Las moléculas se encuentran a grandes distancias entre ellas. En condiciones normales, no hay fuerzas de atracción ni repulsión.
- Al aumentar la temperatura, también aumenta la velocidad de las partículas.
- La presión de un gas es el resultado de los choques de las partículas contra las paredes del recipiente.